QUESTION IMAGE
Question
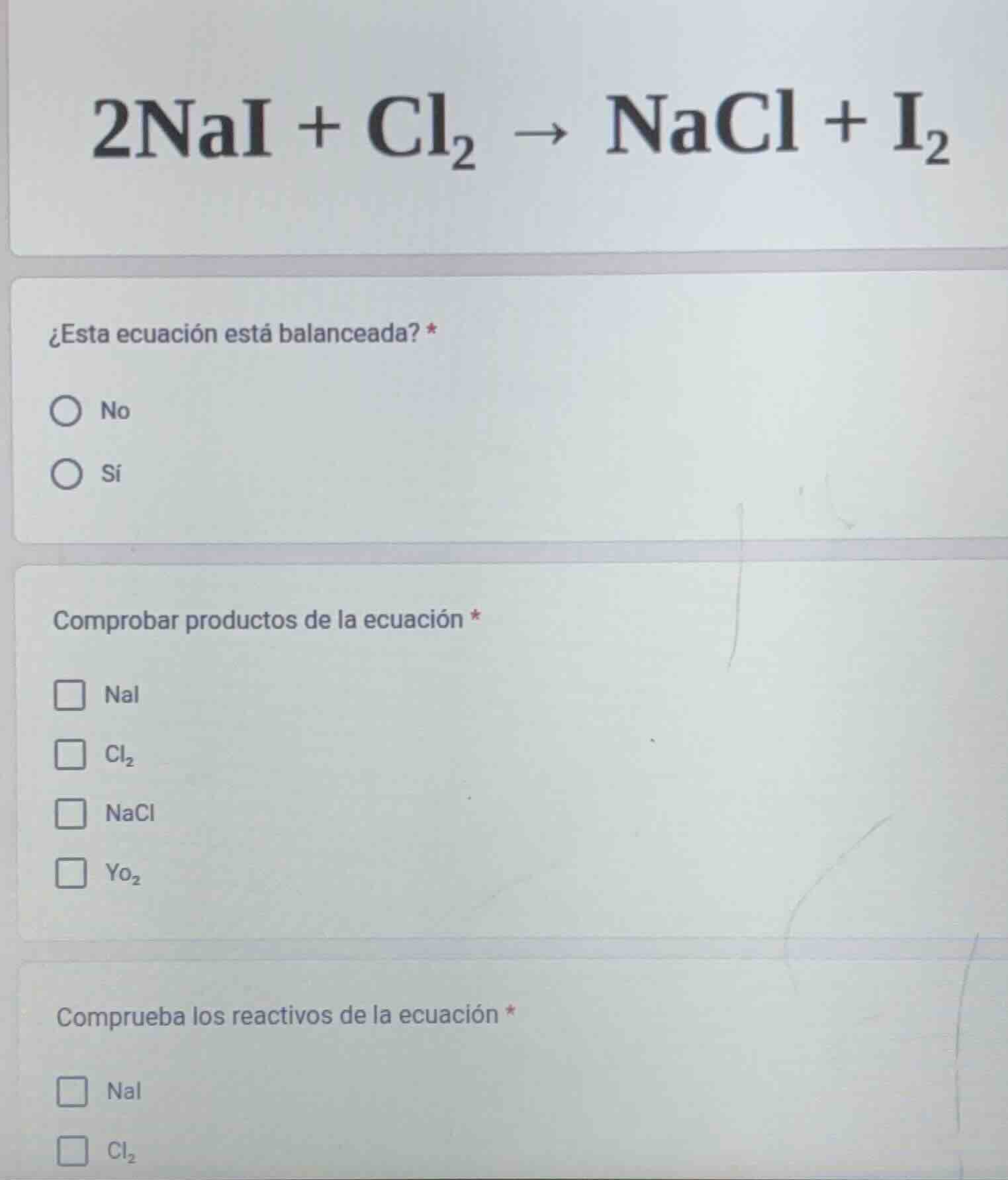
2nai + cl₂ → nacl + i₂
¿esta ecuación está balanceada? *
○ no
○ sí
comprobar productos de la ecuación *
☐ nai
☐ cl₂
☐ nacl
☐ yo₂
comprueba los reactivos de la ecuación *
☐ nai
☐ cl₂
First Sub - Question: ¿Esta ecuación está balanceada?
Para determinar si la ecuación \(2\ce{NaI}+\ce{Cl_2}
ightarrow\ce{NaCl}+\ce{I_2}\) está balanceada, contamos los átomos de cada elemento en los reactantes y en los productos.
- Sodio (Na): En los reactantes, de \(2\ce{NaI}\), hay 2 átomos de Na. En los productos, de \(\ce{NaCl}\), hay 1 átomo de Na (porque la fórmula es \(\ce{NaCl}\) y no hay coeficiente en el producto original).
- Yodo (I): En los reactantes, de \(2\ce{NaI}\), hay 2 átomos de I. En los productos, de \(\ce{I_2}\), hay 2 átomos de I.
- Cloro (Cl): En los reactantes, de \(\ce{Cl_2}\), hay 2 átomos de Cl. En los productos, de \(\ce{NaCl}\), hay 1 átomo de Cl (porque la fórmula es \(\ce{NaCl}\) y no hay coeficiente en el producto original).
Como el número de átomos de Na y Cl no es el mismo en reactantes y productos, la ecuación no está balanceada.
En una ecuación química, los productos son las sustancias que se forman después de la reacción, es decir, los que están a la derecha de la flecha (\(
ightarrow\)). En la ecuación \(2\ce{NaI}+\ce{Cl_2}
ightarrow\ce{NaCl}+\ce{I_2}\), los productos son \(\ce{NaCl}\) y \(\ce{I_2}\). \(\ce{NaI}\) y \(\ce{Cl_2}\) son reactantes (a la izquierda de la flecha), y \(\ce{Yo_2}\) no es un producto de esta reacción.
En una ecuación química, los reactantes son las sustancias que reaccionan, es decir, las que están a la izquierda de la flecha (\(
ightarrow\)). En la ecuación \(2\ce{NaI}+\ce{Cl_2}
ightarrow\ce{NaCl}+\ce{I_2}\), los reactantes son \(\ce{NaI}\) y \(\ce{Cl_2}\).
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
A. No