QUESTION IMAGE
Question
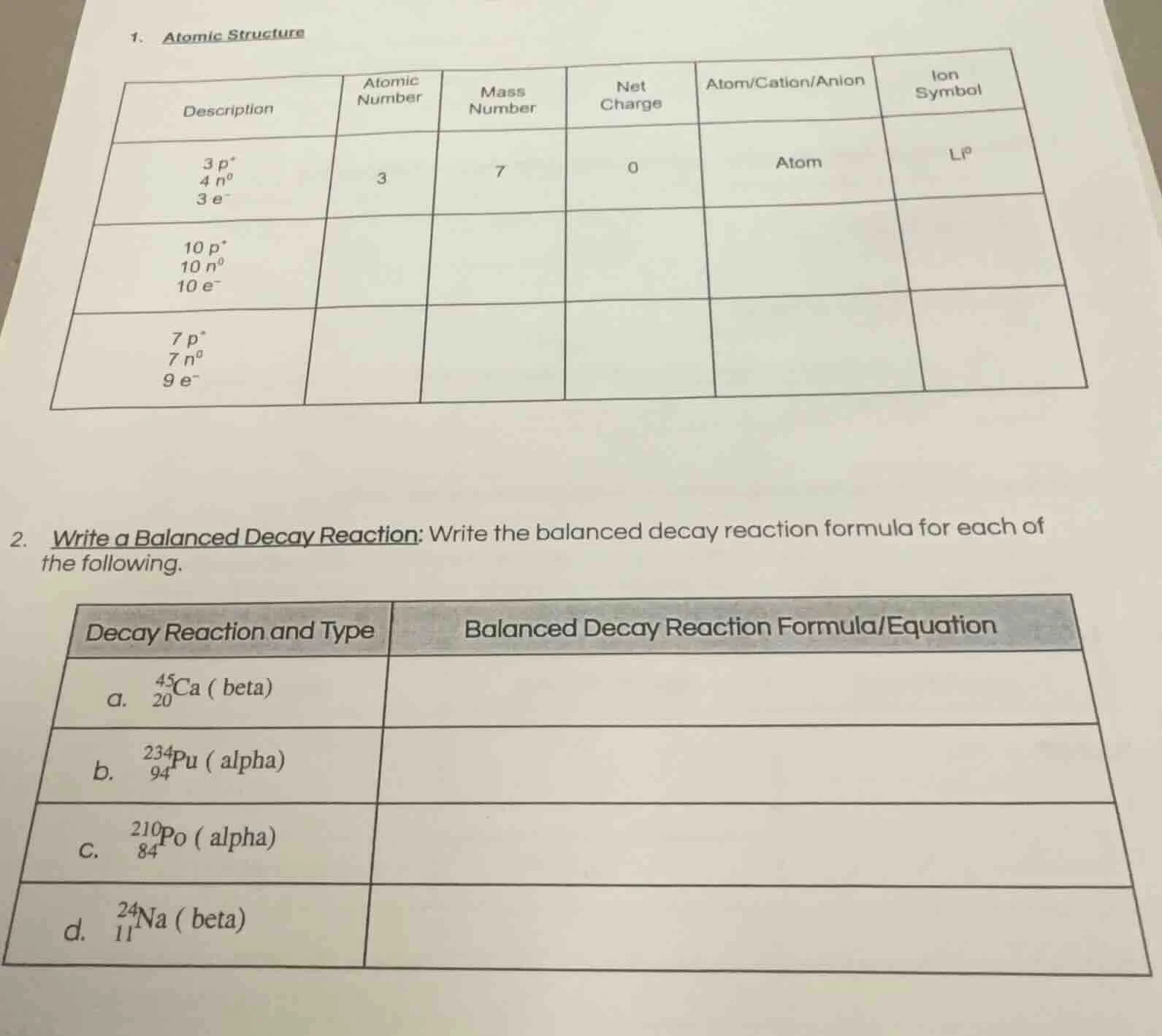
- atomic structure
| description | atomic number | mass number | net charge | atom/cation/anion | ion symbol |
|---|---|---|---|---|---|
| $10\\ p^+$<br>$10\\ n^0$<br>$10\\ e^-$ | |||||
| $7\\ p^+$<br>$7\\ n^0$<br>$9\\ e^-$ |
- write a balanced decay reaction: write the balanced decay reaction formula for each of the following.
| decay reaction and type | balanced decay reaction formula/equation |
|---|---|
| b. $\ce{_{94}^{234}pu}$ (alpha) | |
| c. $\ce{_{84}^{210}po}$ (alpha) | |
| d. $\ce{_{11}^{24}na}$ (beta) |
---
Parte 1: Estructura Atómica
Paso 1: Calcular número atómico
El número atómico es igual al número de protones ($p^+$).
Paso 2: Calcular número de masa
El número de masa es la suma de protones y neutrones ($n^0$): $\text{Número de masa} = p^+ + n^0$
Paso 3: Calcular carga neta
La carga neta es la diferencia entre protones y electrones ($e^-$): $\text{Carga neta} = p^+ - e^-$
Paso 4: Clasificar como átomo/catión/anión
- Átomo: $p^+ = e^-$
- Catión: $p^+ > e^-$ (carga positiva)
- Anión: $p^+ < e^-$ (carga negativa)
Paso 5: Escribir símbolo del ion/átomo
Formato: $\ce{^{A}_{Z}X^{q}}$, donde $Z$ = número atómico, $A$ = número de masa, $q$ = carga neta.
Fila 2 (10 $p^+$, 10 $n^0$, 10 $e^-$):
Paso1: Número atómico
$Z = 10$
Paso2: Número de masa
$A = 10 + 10 = 20$
Paso3: Carga neta
$10 - 10 = 0$
Paso4: Clasificación
Átomo (iguales protones y electrones)
Paso5: Símbolo del átomo
$\ce{^{20}_{10}Ne^0}$
Fila 3 (7 $p^+$, 7 $n^0$, 9 $e^-$):
Paso1: Número atómico
$Z = 7$
Paso2: Número de masa
$A = 7 + 7 = 14$
Paso3: Carga neta
$7 - 9 = -2$
Paso4: Clasificación
Anión (carga negativa)
Paso5: Símbolo del anión
$\ce{^{14}_{7}N^{2-}}$
---
Parte 2: Reacciones de Desintegración Equilibradas
Paso 1: Desintegración beta ($\beta^-$)
Se emite un electrón ($\ce{^{0}_{-1}e}$), el número atómico aumenta en 1, la masa se mantiene:
$\ce{^{A}_{Z}X -> ^{A}_{Z+1}Y + ^{0}_{-1}e}$
Paso 2: Desintegración alfa ($\alpha$)
Se emite un núcleo de helio ($\ce{^{4}_{2}He}$), el número atómico disminuye en 2, la masa en 4:
$\ce{^{A}_{Z}X -> ^{A-4}_{Z-2}Y + ^{4}_{2}He}$
a. $\ce{^{45}_{20}Ca}$ (beta):
Paso1: Aplicar regla de beta
$Z+1=20+1=21$ (elemento Scandio, Sc), $A=45$
$\ce{^{45}_{20}Ca -> ^{45}_{21}Sc + ^{0}_{-1}e}$
b. $\ce{^{234}_{94}Pu}$ (alfa):
Paso1: Aplicar regla de alfa
$Z-2=94-2=92$ (elemento Uranio, U), $A-4=234-4=230$
$\ce{^{234}_{94}Pu -> ^{230}_{92}U + ^{4}_{2}He}$
c. $\ce{^{210}_{84}Po}$ (alfa):
Paso1: Aplicar regla de alfa
$Z-2=84-2=82$ (elemento Plomo, Pb), $A-4=210-4=206$
$\ce{^{210}_{84}Po -> ^{206}_{82}Pb + ^{4}_{2}He}$
d. $\ce{^{24}_{11}Na}$ (beta):
Paso1: Aplicar regla de beta
$Z+1=11+1=12$ (elemento Magnesio, Mg), $A=24$
$\ce{^{24}_{11}Na -> ^{24}_{12}Mg + ^{0}_{-1}e}$
---
Respuesta Final:
1. Tabla de Estructura Atómica
| Description | Atomic Number | Mass Number | Net Charge | Atom/Cation/Anion | Ion Symbol |
|---|---|---|---|---|---|
| 10 $p^+$, 10 $n^0$, 10 $e^-$ | 10 | 20 | 0 | Atom | $\ce{^{20}_{10}Ne^0}$ |
| 7 $p^+$, 7 $n^0$, 9 $e^-$ | 7 | 14 | -2 | Anion | $\ce{^{14}_{7}N^{2-}}$ |
2. Reacciones de Desintegración Equilibradas
a. $\ce{^{45}_{20}Ca -> ^{45}_{21}Sc + ^{0}_{-1}e}$
b. $\ce{^{234}_{94}Pu -> ^{230}_{92}U + ^{4}_{2}He}$
c. $\ce{^{210}_{84}Po -> ^{206}_{82}Pb + ^{4}_{2}He}$
d. $\ce{^{24}_{11}Na -> ^{24}_{12}Mg + ^{0}_{-1}e}$
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
---
Parte 1: Estructura Atómica
Paso 1: Calcular número atómico
El número atómico es igual al número de protones ($p^+$).
Paso 2: Calcular número de masa
El número de masa es la suma de protones y neutrones ($n^0$): $\text{Número de masa} = p^+ + n^0$
Paso 3: Calcular carga neta
La carga neta es la diferencia entre protones y electrones ($e^-$): $\text{Carga neta} = p^+ - e^-$
Paso 4: Clasificar como átomo/catión/anión
- Átomo: $p^+ = e^-$
- Catión: $p^+ > e^-$ (carga positiva)
- Anión: $p^+ < e^-$ (carga negativa)
Paso 5: Escribir símbolo del ion/átomo
Formato: $\ce{^{A}_{Z}X^{q}}$, donde $Z$ = número atómico, $A$ = número de masa, $q$ = carga neta.
Fila 2 (10 $p^+$, 10 $n^0$, 10 $e^-$):
Paso1: Número atómico
$Z = 10$
Paso2: Número de masa
$A = 10 + 10 = 20$
Paso3: Carga neta
$10 - 10 = 0$
Paso4: Clasificación
Átomo (iguales protones y electrones)
Paso5: Símbolo del átomo
$\ce{^{20}_{10}Ne^0}$
Fila 3 (7 $p^+$, 7 $n^0$, 9 $e^-$):
Paso1: Número atómico
$Z = 7$
Paso2: Número de masa
$A = 7 + 7 = 14$
Paso3: Carga neta
$7 - 9 = -2$
Paso4: Clasificación
Anión (carga negativa)
Paso5: Símbolo del anión
$\ce{^{14}_{7}N^{2-}}$
---
Parte 2: Reacciones de Desintegración Equilibradas
Paso 1: Desintegración beta ($\beta^-$)
Se emite un electrón ($\ce{^{0}_{-1}e}$), el número atómico aumenta en 1, la masa se mantiene:
$\ce{^{A}_{Z}X -> ^{A}_{Z+1}Y + ^{0}_{-1}e}$
Paso 2: Desintegración alfa ($\alpha$)
Se emite un núcleo de helio ($\ce{^{4}_{2}He}$), el número atómico disminuye en 2, la masa en 4:
$\ce{^{A}_{Z}X -> ^{A-4}_{Z-2}Y + ^{4}_{2}He}$
a. $\ce{^{45}_{20}Ca}$ (beta):
Paso1: Aplicar regla de beta
$Z+1=20+1=21$ (elemento Scandio, Sc), $A=45$
$\ce{^{45}_{20}Ca -> ^{45}_{21}Sc + ^{0}_{-1}e}$
b. $\ce{^{234}_{94}Pu}$ (alfa):
Paso1: Aplicar regla de alfa
$Z-2=94-2=92$ (elemento Uranio, U), $A-4=234-4=230$
$\ce{^{234}_{94}Pu -> ^{230}_{92}U + ^{4}_{2}He}$
c. $\ce{^{210}_{84}Po}$ (alfa):
Paso1: Aplicar regla de alfa
$Z-2=84-2=82$ (elemento Plomo, Pb), $A-4=210-4=206$
$\ce{^{210}_{84}Po -> ^{206}_{82}Pb + ^{4}_{2}He}$
d. $\ce{^{24}_{11}Na}$ (beta):
Paso1: Aplicar regla de beta
$Z+1=11+1=12$ (elemento Magnesio, Mg), $A=24$
$\ce{^{24}_{11}Na -> ^{24}_{12}Mg + ^{0}_{-1}e}$
---
Respuesta Final:
1. Tabla de Estructura Atómica
| Description | Atomic Number | Mass Number | Net Charge | Atom/Cation/Anion | Ion Symbol |
|---|---|---|---|---|---|
| 10 $p^+$, 10 $n^0$, 10 $e^-$ | 10 | 20 | 0 | Atom | $\ce{^{20}_{10}Ne^0}$ |
| 7 $p^+$, 7 $n^0$, 9 $e^-$ | 7 | 14 | -2 | Anion | $\ce{^{14}_{7}N^{2-}}$ |
2. Reacciones de Desintegración Equilibradas
a. $\ce{^{45}_{20}Ca -> ^{45}_{21}Sc + ^{0}_{-1}e}$
b. $\ce{^{234}_{94}Pu -> ^{230}_{92}U + ^{4}_{2}He}$
c. $\ce{^{210}_{84}Po -> ^{206}_{82}Pb + ^{4}_{2}He}$
d. $\ce{^{24}_{11}Na -> ^{24}_{12}Mg + ^{0}_{-1}e}$