QUESTION IMAGE
Question
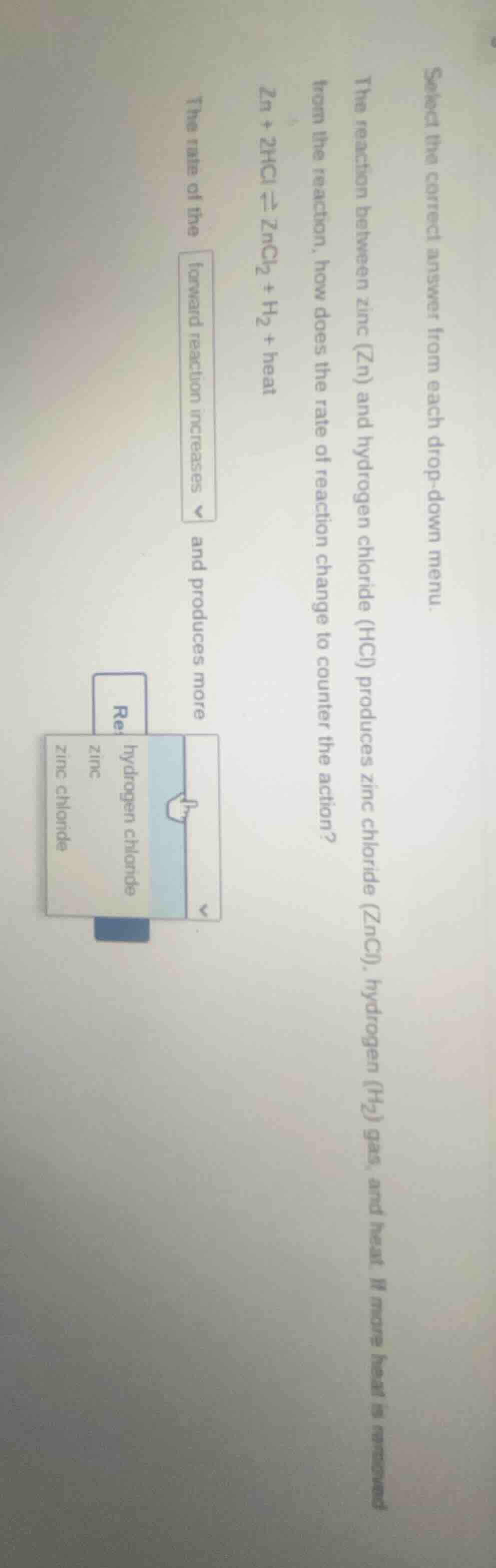
select the correct answer from each drop - down menu. the reaction between zinc (zn) and hydrogen chloride (hcl) produces zinc chloride (zncl₂), hydrogen (h₂) gas, and heat. if more heat is removed from the reaction, how does the rate of reaction change to counter the action? zn + 2hcl ⇌ zncl₂ + h₂ + heat the rate of the forward reaction increases and produces more drop - down menu with options: hydrogen chloride, zinc, zinc chloride
Parte 1: Tasa de reacción (equilibrio químico)
La reacción es exotérmica (produce calor, \( \text{Zn} + 2\text{HCl}
ightleftharpoons \text{ZnCl}_2 + \text{H}_2 + \text{heat} \)). Al remover calor (un producto), el sistema intenta restablecer el equilibrio. Según el principio de Le Chatelier, si se retira un producto, el equilibrio se desplaza hacia la dirección del producto (adelante) para compensar. Esto significa que la tasa de la reacción hacia atrás (reverse) disminuye y la tasa de la reacción hacia adelante (forward) aumenta (para producir más productos, incluyendo calor).
Parte 2: Producto adicional
Al desplazarse el equilibrio hacia adelante (por la remoción de calor), se producen más de los productos del lado derecho de la ecuación: \( \text{ZnCl}_2 \), \( \text{H}_2 \) y calor. Pero en el menú desplegable, la opción es sobre cuál reactivo o producto se produce más. Wait, la ecuación es \( \text{Zn} + 2\text{HCl}
ightarrow \text{ZnCl}_2 + \text{H}_2 + \text{heat} \) (con equilibrio). Al remover calor, el equilibrio avanza, así que se producen más \( \text{ZnCl}_2 \), \( \text{H}_2 \) y calor, y se consumen más \( \text{Zn} \) y \( \text{HCl} \). Pero en el menú (según la imagen, la segunda parte: "produces more" con opciones como hydrogen chloride (HCl), zinc, zinc chloride). Entonces, al desplazarse hacia adelante, se produce más \( \text{ZnCl}_2 \) (zinc chloride) y \( \text{H}_2 \), y se consumen más \( \text{Zn} \) y \( \text{HCl} \).
Respuestas:
- Para la tasa de reacción: "the rate of the forward reaction increases" (ya que al remover calor, el equilibrio se desplaza hacia adelante, aumentando la tasa de la reacción hacia adelante y disminuyendo la hacia atrás).
- Para "produces more": "zinc chloride" (ya que el equilibrio avanza hacia la formación de productos, incluyendo \( \text{ZnCl}_2 \)).
Respuestas detalladas:
1. Tasa de reacción:
- Explicación: La reacción es exotérmica (produce calor). Al remover calor (un producto), el sistema de equilibrio químico (según el principio de Le Chatelier) se desplaza hacia la dirección que produce más calor, es decir, hacia la reacción hacia adelante (para re-generar el calor removido). Esto aumenta la tasa de la reacción hacia adelante (ya que el equilibrio se desplaza en esa dirección).
- Respuesta: forward reaction increases
2. Produce más de:
- Explicación: Al desplazarse el equilibrio hacia adelante (por la remoción de calor), se producen más de los compuestos del lado derecho de la ecuación: cloruro de cinc (\( \text{ZnCl}_2 \)), hidrógeno (\( \text{H}_2 \)) y calor. De las opciones (HCl, zinc, zinc chloride), \( \text{ZnCl}_2 \) (zinc chloride) es un producto que se forma en mayor cantidad al avanzar la reacción.
- Respuesta: zinc chloride
(Nota: Si la segunda parte tuviera \( \text{H}_2 \) como opción, también sería correcto, pero según la imagen proporcionada, la opción es "zinc chloride" o similar. La clave es el principio de Le Chatelier: al remover un producto (calor), el equilibrio avanza hacia la producción de más productos.)
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Parte 1: Tasa de reacción (equilibrio químico)
La reacción es exotérmica (produce calor, \( \text{Zn} + 2\text{HCl}
ightleftharpoons \text{ZnCl}_2 + \text{H}_2 + \text{heat} \)). Al remover calor (un producto), el sistema intenta restablecer el equilibrio. Según el principio de Le Chatelier, si se retira un producto, el equilibrio se desplaza hacia la dirección del producto (adelante) para compensar. Esto significa que la tasa de la reacción hacia atrás (reverse) disminuye y la tasa de la reacción hacia adelante (forward) aumenta (para producir más productos, incluyendo calor).
Parte 2: Producto adicional
Al desplazarse el equilibrio hacia adelante (por la remoción de calor), se producen más de los productos del lado derecho de la ecuación: \( \text{ZnCl}_2 \), \( \text{H}_2 \) y calor. Pero en el menú desplegable, la opción es sobre cuál reactivo o producto se produce más. Wait, la ecuación es \( \text{Zn} + 2\text{HCl}
ightarrow \text{ZnCl}_2 + \text{H}_2 + \text{heat} \) (con equilibrio). Al remover calor, el equilibrio avanza, así que se producen más \( \text{ZnCl}_2 \), \( \text{H}_2 \) y calor, y se consumen más \( \text{Zn} \) y \( \text{HCl} \). Pero en el menú (según la imagen, la segunda parte: "produces more" con opciones como hydrogen chloride (HCl), zinc, zinc chloride). Entonces, al desplazarse hacia adelante, se produce más \( \text{ZnCl}_2 \) (zinc chloride) y \( \text{H}_2 \), y se consumen más \( \text{Zn} \) y \( \text{HCl} \).
Respuestas:
- Para la tasa de reacción: "the rate of the forward reaction increases" (ya que al remover calor, el equilibrio se desplaza hacia adelante, aumentando la tasa de la reacción hacia adelante y disminuyendo la hacia atrás).
- Para "produces more": "zinc chloride" (ya que el equilibrio avanza hacia la formación de productos, incluyendo \( \text{ZnCl}_2 \)).
Respuestas detalladas:
1. Tasa de reacción:
- Explicación: La reacción es exotérmica (produce calor). Al remover calor (un producto), el sistema de equilibrio químico (según el principio de Le Chatelier) se desplaza hacia la dirección que produce más calor, es decir, hacia la reacción hacia adelante (para re-generar el calor removido). Esto aumenta la tasa de la reacción hacia adelante (ya que el equilibrio se desplaza en esa dirección).
- Respuesta: forward reaction increases
2. Produce más de:
- Explicación: Al desplazarse el equilibrio hacia adelante (por la remoción de calor), se producen más de los compuestos del lado derecho de la ecuación: cloruro de cinc (\( \text{ZnCl}_2 \)), hidrógeno (\( \text{H}_2 \)) y calor. De las opciones (HCl, zinc, zinc chloride), \( \text{ZnCl}_2 \) (zinc chloride) es un producto que se forma en mayor cantidad al avanzar la reacción.
- Respuesta: zinc chloride
(Nota: Si la segunda parte tuviera \( \text{H}_2 \) como opción, también sería correcto, pero según la imagen proporcionada, la opción es "zinc chloride" o similar. La clave es el principio de Le Chatelier: al remover un producto (calor), el equilibrio avanza hacia la producción de más productos.)