QUESTION IMAGE
Question
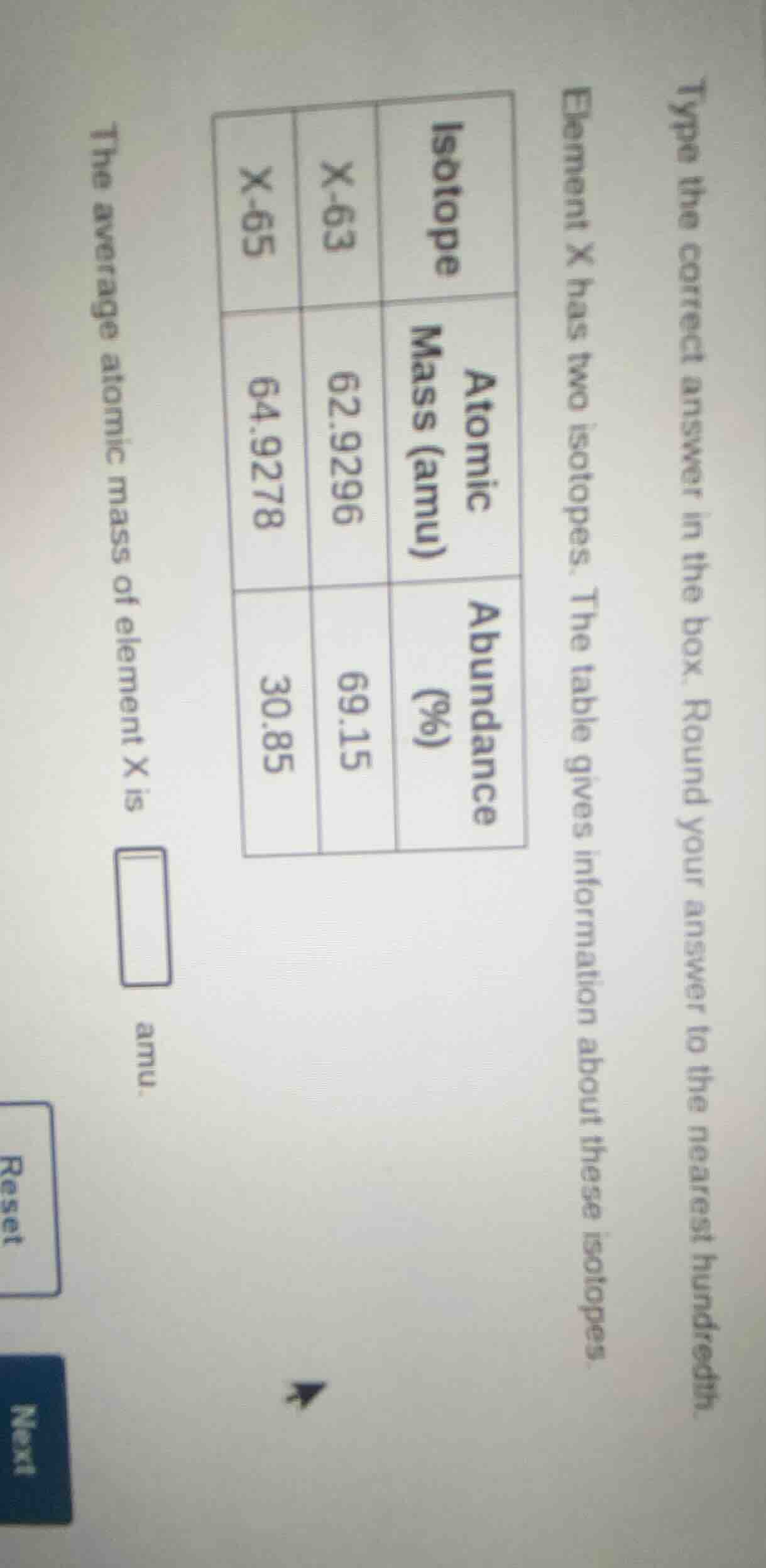
type the correct answer in the box. round your answer to the nearest hundredth. element x has two isotopes. the table gives information about these isotopes. isotope atomic mass (amu) abundance (%) x-63 62.9296 69.15 x-65 64.9278 30.85 the average atomic mass of element x is amu.
Step1: Calcular el producto de la masa y la abundancia para X-63
Multiplicamos la masa del isótopo X-63 (62.9296 amu) por su abundancia (69.15% o 0.6915 en decimal):
$62.9296 \times 0.6915$
Step2: Calcular el producto de la masa y la abundancia para X-65
Multiplicamos la masa del isótopo X-65 (64.9278 amu) por su abundancia (30.85% o 0.3085 en decimal):
$64.9278 \times 0.3085$
Step3: Sumar los dos productos para obtener la masa atómica promedio
Sumamos los resultados de los pasos 1 y 2:
$(62.9296 \times 0.6915) + (64.9278 \times 0.3085)$
Calculando cada término:
- Para X-63: $62.9296 \times 0.6915 \approx 43.515$
- Para X-65: $64.9278 \times 0.3085 \approx 20.030$
Suma: $43.515 + 20.030 = 63.545$ (redondeado a dos decimales: 63.55)
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
63.55