QUESTION IMAGE
Question
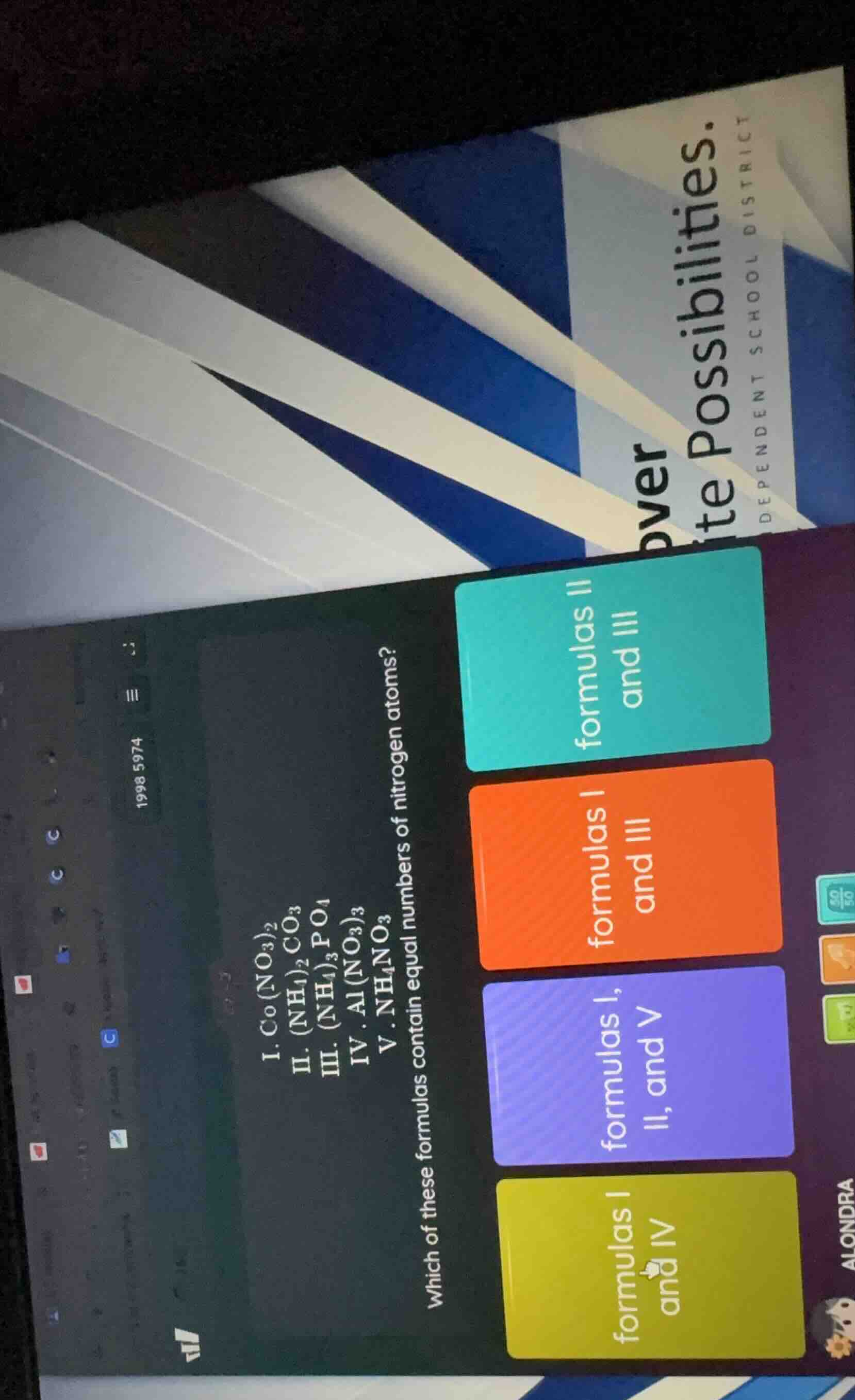
i. co(no₃)₂
ii. (nh₄)₂co₃
iii. (nh₄)₃po₄
iv. al(no₃)₃
v. nh₄no₃
which of these formulas contain equal numbers of nitrogen atoms?
formulas ii and iii
formulas i and iii
formulas i, ii, and v
formulas i and iv
Step1: Analizar cada fórmula
- Fórmula I: $\ce{Co(NO_{3})_{2}}$
En $\ce{NO_{3}^-}$ (ion nitrato), hay 1 átomo de N por ion. El coeficiente del ion es 2, así que el número de átomos de N es $1\times2 = 2$.
- Fórmula II: $\ce{(NH_{4})_{2}CO_{3}}$
En $\ce{NH_{4}^+}$ (ion amonio), hay 1 átomo de N por ion. El coeficiente del ion es 2, así que el número de átomos de N es $1\times2 = 2$.
- Fórmula III: $\ce{(NH_{4})_{3}PO_{4}}$
En $\ce{NH_{4}^+}$, hay 1 átomo de N por ion. El coeficiente del ion es 3, así que el número de átomos de N es $1\times3 = 3$.
- Fórmula IV: $\ce{Al(NO_{3})_{3}}$
En $\ce{NO_{3}^-}$, hay 1 átomo de N por ion. El coeficiente del ion es 3, así que el número de átomos de N es $1\times3 = 3$.
- Fórmula V: $\ce{NH_{4}NO_{3}}$
Tiene dos grupos con N: $\ce{NH_{4}^+}$ (1 átomo de N) y $\ce{NO_{3}^-}$ (1 átomo de N). Total de átomos de N: $1 + 1 = 2$.
Step2: Comparar cantidades de N
- Fórmula I: 2 átomos de N
- Fórmula II: 2 átomos de N
- Fórmula V: 2 átomos de N
- Fórmula III: 3 átomos de N
- Fórmula IV: 3 átomos de N
Las fórmulas con la misma cantidad de átomos de N son I, II y V (todas con 2 átomos de N), y III y IV (todas con 3 átomos de N). Pero la opción que incluye I, II y V es la que tiene cantidades iguales entre ellas.
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
formulas I, II, and V