QUESTION IMAGE
Question
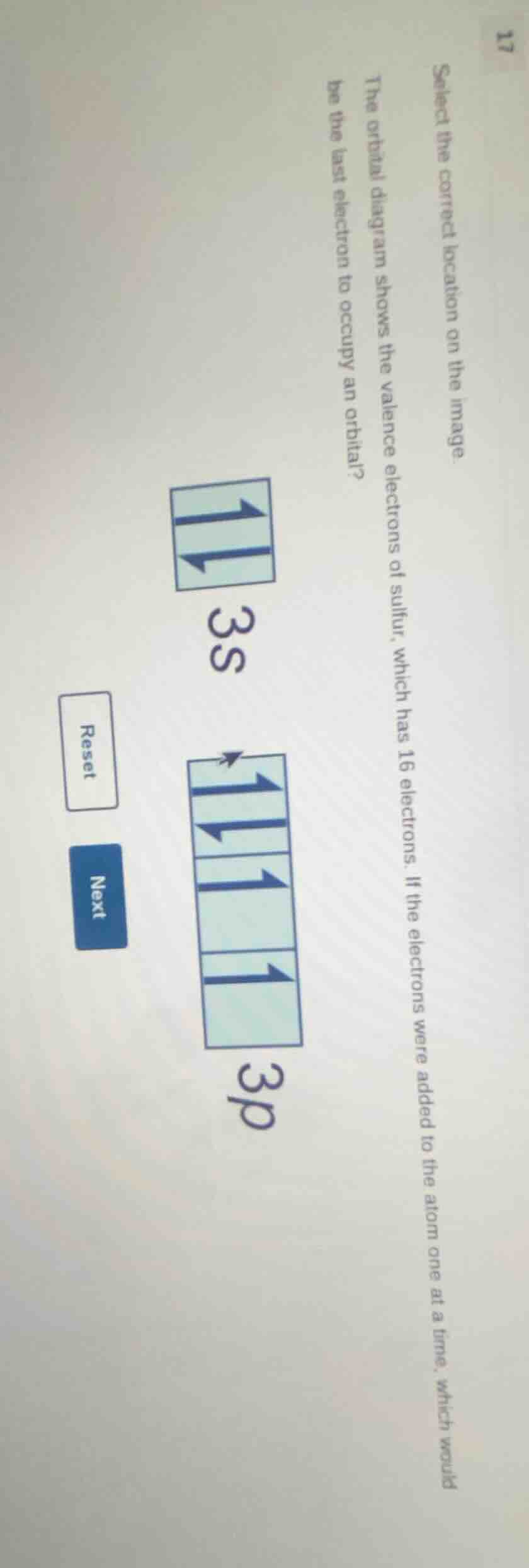
select the correct location on the image. the orbital diagram shows the valence electrons of sulfur, which has 16 electrons. if the electrons were added to the atom one at a time, which would be the last electron to occupy an orbital?
Step1: Recuerda la configuración electrónica del azufre (S). El número atómico del azufre es 16, por lo que su configuración electrónica es \(1s^2 2s^2 2p^6 3s^2 3p^4\).
Step2: Analiza los orbitales de valencia. Los electrones de valencia del azufre están en el nivel 3: \(3s^2\) y \(3p^4\). Primero se llenan los orbitales \(3s\) (con 2 electrones) y luego los \(3p\).
Step3: Llenado de orbitales \(3p\). Los orbitales \(p\) tienen 3 suborbitales, y se llena siguiendo el principio de Hund: primero se colocan electrones con espín paralelo en cada suborbital antes de emparejar. Para \(3p^4\), los primeros 3 electrones ocupan cada suborbital \(3p\) con espín hacia arriba, y el cuarto (el último en llenar el \(3p\)) empareja en uno de los suborbitales \(3p\) que ya tiene un electrón (con espín hacia abajo). Observando el diagrama, el \(3p\) tiene tres suborbitales; el último electrón (el 16º) ocupará el suborbital \(3p\) que aún no está completamente lleno (el que tiene solo un electrón con espín hacia arriba, y se le agrega uno con espín hacia abajo). En el diagrama mostrado, el suborbital \(3p\) que es el segundo (o el que tiene el espacio para el segundo electrón) sería donde va el último electrón. Pero más precisamente, la configuración \(3p^4\) significa que después de llenar los tres suborbitales \(3p\) con un electrón cada uno (hasta \(3p^3\)), el cuarto electrón (el último en el \(3p\)) empareja en uno de esos suborbitales. Entonces, el último electrón para el azufre (el 16º) ocupará el suborbital \(3p\) que ya tiene un electrón (el que se indica con la flecha en el diagrama, probablemente el suborbital \(3p\) que es el segundo o el que está en el medio o el que tiene el espacio para el segundo electrón).
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
El último electrón para el azufre (con 16 electrones) ocupará el suborbital \(3p\) (en el diagrama, el suborbital \(3p\) que es el segundo o el que tiene la flecha, donde se empareja el electrón). En términos del diagrama mostrado, el lugar correcto es el suborbital \(3p\) que es el segundo (o el que está en el medio de los tres suborbitales \(3p\)) para emparejar el electrón (ya que \(3p^4\) implica que uno de los suborbitales \(3p\) tiene dos electrones y los otros dos tienen uno cada uno; el último electrón va a emparejar en uno de los suborbitales \(3p\) que tenía un electrón).