QUESTION IMAGE
Question
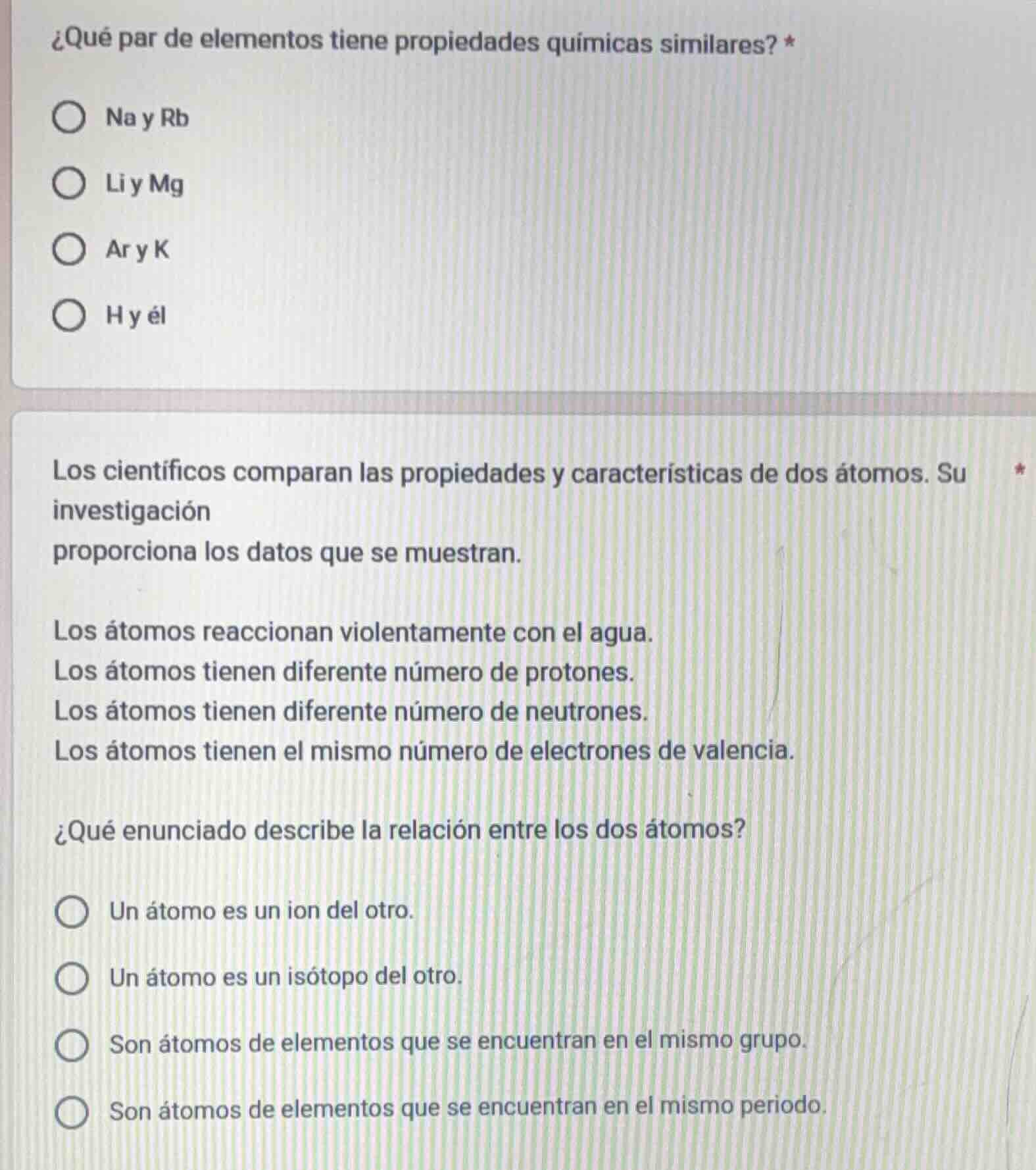
¿qué par de elementos tiene propiedades químicas similares? *
na y rb
li y mg
ar y k
h y él
los científicos comparan las propiedades y características de dos átomos. su investigación
proporciona los datos que se muestran.
los átomos reaccionan violentamente con el agua.
los átomos tienen diferente número de protones.
los átomos tienen diferente número de neutrones.
los átomos tienen el mismo número de electrones de valencia.
¿qué enunciado describe la relación entre los dos átomos?
un átomo es un ion del otro.
un átomo es un isótopo del otro.
son átomos de elementos que se encuentran en el mismo grupo.
son átomos de elementos que se encuentran en el mismo periodo.
First Question (¿Qué par de elementos tiene propiedades químicas similares?):
Elementos en el mismo grupo de la tabla periódica tienen propiedades químicas similares. Na (sodio) y Rb (rubidio) pertenecen al grupo 1 (metales alcalinos). Li (litio) está en grupo 1, Mg (magnesio) en grupo 2; Ar (argón) es gas noble (grupo 18), K (potasio) grupo 1; H (hidrógeno) no es metal alcalino, y "él" no es un elemento. Entonces Na y Rb son del mismo grupo.
- Ión: Cambia número de electrones, no valencia (aquí mismo número de electrones de valencia).
- Isótopo: Mismo número de protones, distinto de neutrones (aquí distinto número de protones, así que no).
- Mismo grupo: Elementos en el mismo grupo tienen mismo número de electrones de valencia, reacciones similares (como reaccionar violentamente con agua, típico de grupo 1). Distinto número de protones (diferente elemento), mismo grupo implica mismo número de electrones de valencia.
- Mismo período: No garantiza mismo número de electrones de valencia.
Entonces la relación es que son átomos de elementos del mismo grupo.
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
A. Na y Rb