QUESTION IMAGE
Question
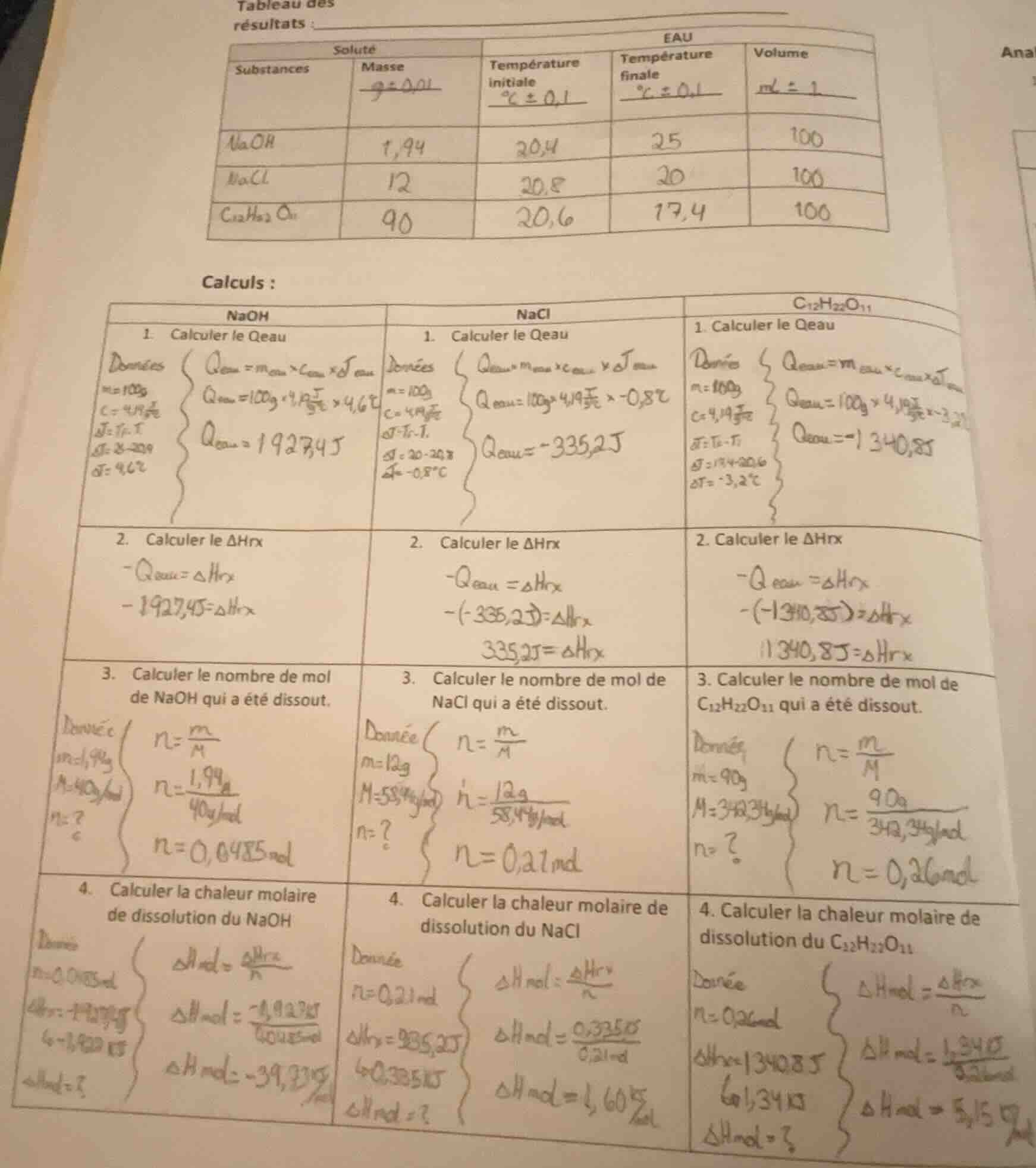
tableau des
résultats :
| substances | solute (masse, g ± 0.01) | température initiale (°c ± 0.1) | eau (température finale, °c ± 0.1) | eau (volume, ml ± 1) |
|---|---|---|---|---|
| nacl | 12 | 20,8 | 20 | 100 |
| c₁₂h₂₂o₁₁ | 90 | 20,6 | 17,4 | 100 |
calculs :
naoh
- calculer le qeau
données :
- ( m = 100g )
- ( c = 4,19 \frac{j}{gcdot^circ c} )
- ( delta t = t_f - t_i = 25 - 20,4 = 4,6^circ c )
formule : ( q_{eau} = m_{eau} \times c_{eau} \times delta t_{eau} )
calcul : ( q_{eau} = 100g \times 4,19 \frac{j}{gcdot^circ c} \times 4,6^circ c = 1927,4j )
- calculer le ( delta h_{rx} )
formule : ( -!q_{eau} = delta h_{rx} )
calcul : ( -!1927,4j = delta h_{rx} )
- calculer le nombre de mol de naoh qui a été dissout.
données :
- ( m = 1,94g )
- ( m = 40g/mol )
formule : ( n = \frac{m}{m} )
calcul : ( n = \frac{1,94g}{40g/mol} = 0,0485mol )
- calculer la chaleur molaire de dissolution du naoh
formule : ( delta h_{mol} = \frac{delta h_{rx}}{n} )
calcul : ( delta h_{mol} = \frac{-1927,4j}{0,0485mol} approx -39740j/mol = -39,74kj/mol )
nacl
- calculer le qeau
données :
- ( m = 100g )
- ( c = 4,19 \frac{j}{gcdot^circ c} )
- ( delta t = t_f - t_i = 20 - 20,8 = -0,8^circ c )
formule : ( q_{eau} = m_{eau} \times c_{eau} \times delta t_{eau} )
calcul : ( q_{eau} = 100g \times 4,19 \frac{j}{gcdot^circ c} \times (-0,8)^circ c = -335,2j )
- calculer le ( delta h_{rx} )
formule : ( -!q_{eau} = delta h_{rx} )
calcul : ( -!(-335,2j) = delta h_{rx} implies 335,2j = delta h_{rx} )
- calculer le nombre de mol de nacl qui a été dissout.
données :
- ( m = 12g )
- ( m = 58,44g/mol )
formule : ( n = \frac{m}{m} )
calcul : ( n = \frac{12g}{58,44g/mol} approx 0,205mol ) (note: original calculation shows 0,21mol, likely rounding)
- calculer la chaleur molaire de dissolution du nacl
formule : ( delta h_{mol} = \frac{delta h_{rx}}{n} )
calcul : ( delta h_{mol} = \frac{335,2j}{0,205mol} approx 1635j/mol approx 1,64kj/mol ) (note: original calculation shows 1,60kj/mol, likely rounding)
c₁₂h₂₂o₁₁
- calculer le qeau
données :
- ( m = 100g )
- ( c = 4,19 \frac{j}{gcdot^circ c} )
- ( delta t = t_f - t_i = 17,4 - 20,6 = -3,2^circ c )
formule : ( q_{eau} = m_{eau} \times c_{eau} \times delta t_{eau} )
calcul : ( q_{eau} = 100g \times 4,19 \frac{j}{gcdot^circ c} \times (-3,2)^circ c = -1340,8j )
- calculer le ( delta h_{rx} )
formule : ( -!q_{eau} = delta h_{rx} )
calcul : ( -!(-1340,8j) = delta h_{rx} implies 1340,8j = delta h_{rx} )
- calculer le nombre de mol de c₁₂h₂₂o₁₁ qui a été dissout.
données :
- ( m = 90g )
- ( m = 342,3g/mol )
formule : ( n = \frac{m}{m} )
calcul : ( n = \frac{90g}{342,3g/mol} approx 0,263mol ) (note: original calculation shows 0,26mol, likely rounding)
- calculer la chaleur molaire de dissolution du c₁₂h₂₂o₁₁
formule : ( delta h_{mol} = \frac{delta h_{rx}}{n} )
calcul : ( delta h_{mol} = \frac{1340,8j}{0,263mol} approx 5098j/mol approx 5,10kj/mol ) (note: original calculation shows 5,15kj/mol, likely rounding)
Step1: Vérifier $Q_{eau}$ (NaOH)
Formule : $Q_{eau} = m_{eau} \times c_{eau} \times \Delta T$
$m_{eau}=100\ \text{g}$, $c_{eau}=4,19\ \frac{\text{J}}{\text{g}^\circ\text{C}}$, $\Delta T=25-20,4=4,6^\circ\text{C}$
$Q_{eau}=100 \times 4,19 \times 4,6 = 1927,4\ \text{J}$
Step2: Vérifier $\Delta H_{rx}$ (NaOH)
Formule : $\Delta H_{rx} = -Q_{eau}$
$\Delta H_{rx}= -1927,4\ \text{J} = -1,9274\ \text{kJ}$
Step3: Vérifier $n$ (NaOH)
Formule : $n = \frac{m}{M}$
$m=1,94\ \text{g}$, $M_{NaOH}=40\ \frac{\text{g}}{\text{mol}}$
$n=\frac{1,94}{40}=0,0485\ \text{mol}$
Step4: Vérifier $\Delta H_{mol}$ (NaOH)
Formule : $\Delta H_{mol} = \frac{\Delta H_{rx}}{n}$
$\Delta H_{mol}=\frac{-1,9274}{0,0485} \approx -39,7\ \frac{\text{kJ}}{\text{mol}}$
---
Step5: Vérifier $Q_{eau}$ (NaCl)
Formule : $Q_{eau} = m_{eau} \times c_{eau} \times \Delta T$
$\Delta T=20-20,8=-0,8^\circ\text{C}$
$Q_{eau}=100 \times 4,19 \times (-0,8) = -335,2\ \text{J}$
Step6: Vérifier $\Delta H_{rx}$ (NaCl)
$\Delta H_{rx}= -(-335,2)=335,2\ \text{J}=0,3352\ \text{kJ}$
Step7: Vérifier $n$ (NaCl)
$M_{NaCl}=58,44\ \frac{\text{g}}{\text{mol}}$
$n=\frac{12}{58,44}\approx0,205\ \text{mol}$
Step8: Vérifier $\Delta H_{mol}$ (NaCl)
$\Delta H_{mol}=\frac{0,3352}{0,205}\approx1,635\ \frac{\text{kJ}}{\text{mol}}$
---
Step9: Vérifier $Q_{eau}$ (C₁₂H₂₂O₁₁)
Formule : $Q_{eau} = m_{eau} \times c_{eau} \times \Delta T$
$\Delta T=17,4-20,6=-3,2^\circ\text{C}$
$Q_{eau}=100 \times 4,19 \times (-3,2) = -1340,8\ \text{J}$
Step10: Vérifier $\Delta H_{rx}$ (C₁₂H₂₂O₁₁)
$\Delta H_{rx}= -(-1340,8)=1340,8\ \text{J}=1,3408\ \text{kJ}$
Step11: Vérifier $n$ (C₁₂H₂₂O₁₁)
$M_{C_{12}H_{22}O_{11}}=342,3\ \frac{\text{g}}{\text{mol}}$
$n=\frac{90}{342,3}\approx0,263\ \text{mol}$
Step12: Vérifier $\Delta H_{mol}$ (C₁₂H₂₂O₁₁)
$\Delta H_{mol}=\frac{1,3408}{0,263}\approx5,1\ \frac{\text{kJ}}{\text{mol}}$
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Résultats corrigés :
- NaOH
- $Q_{eau}=1927,4\ \text{J}$
- $\Delta H_{rx}=-1,93\ \text{kJ}$
- $n=0,0485\ \text{mol}$
- $\Delta H_{mol}\approx-39,7\ \frac{\text{kJ}}{\text{mol}}$
- NaCl
- $Q_{eau}=-335,2\ \text{J}$
- $\Delta H_{rx}=0,335\ \text{kJ}$
- $n\approx0,205\ \text{mol}$
- $\Delta H_{mol}\approx1,64\ \frac{\text{kJ}}{\text{mol}}$
- C₁₂H₂₂O₁₁
- $Q_{eau}=-1340,8\ \text{J}$
- $\Delta H_{rx}=1,34\ \text{kJ}$
- $n\approx0,263\ \text{mol}$
- $\Delta H_{mol}\approx5,1\ \frac{\text{kJ}}{\text{mol}}$
Les calculs initiaux sont globalement corrects, avec des ajustements de précision sur les masses molaires et les divisions finales.