QUESTION IMAGE
Question
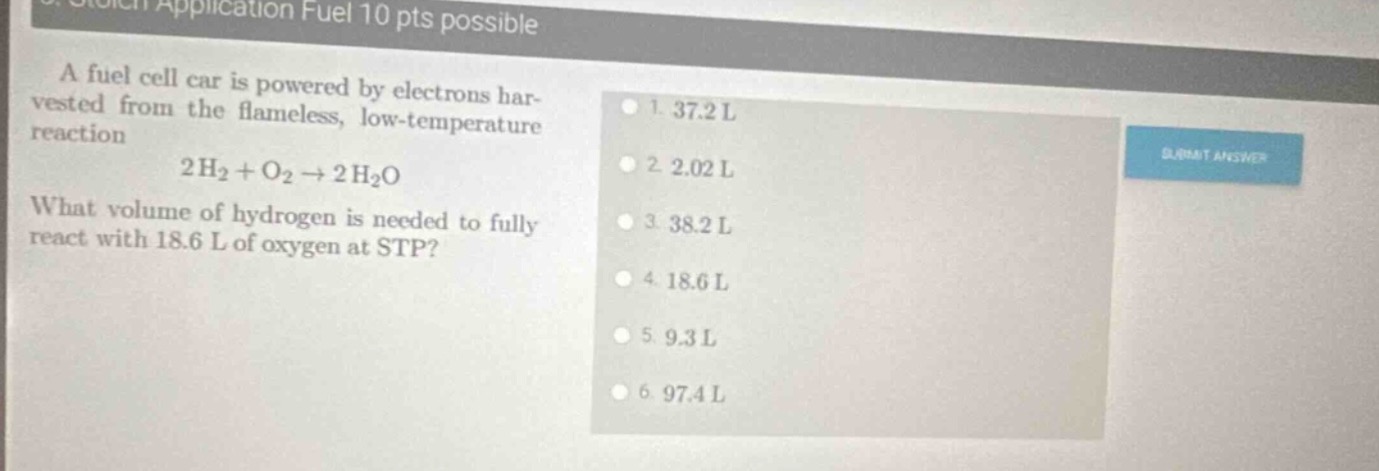
application fuel 10 pts possible a fuel cell car is powered by electrons harvested from the flameless, low - temperature reaction \\(2h_2 + o_2 \
ightarrow 2h_2o\\) what volume of hydrogen is needed to fully react with 18.6 l of oxygen at stp? 1. 37.2 l 2. 2.02 l 3. 38.2 l 4. 18.6 l 5. 9.3 l 6. 97.4 l
Step1: Analizar la ecuación estequiométrica
La reacción es \( 2\text{H}_2 + \text{O}_2
ightarrow 2\text{H}_2\text{O} \). En STP, los volúmenes de gases se relacionan según las proporciones estequiométricas. La relación entre \( \text{H}_2 \) y \( \text{O}_2 \) es 2:1 (2 moles de \( \text{H}_2 \) por 1 mol de \( \text{O}_2 \), y en STP, el volumen de un gas es proporcional a la cantidad de sustancia, así que la relación de volúmenes es la misma que la de moles).
Step2: Aplicar la proporción de volúmenes
Si el volumen de \( \text{O}_2 \) es 18.6 L, y la relación \( \text{H}_2 : \text{O}_2 = 2 : 1 \), entonces el volumen de \( \text{H}_2 \) se calcula como \( \text{Volumen de } \text{H}_2 = 2 \times \text{Volumen de } \text{O}_2 \)
\[
\text{Volumen de } \text{H}_2 = 2 \times 18.6\ \text{L} = 37.2\ \text{L}
\]
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
- 37.2 L