QUESTION IMAGE
Question
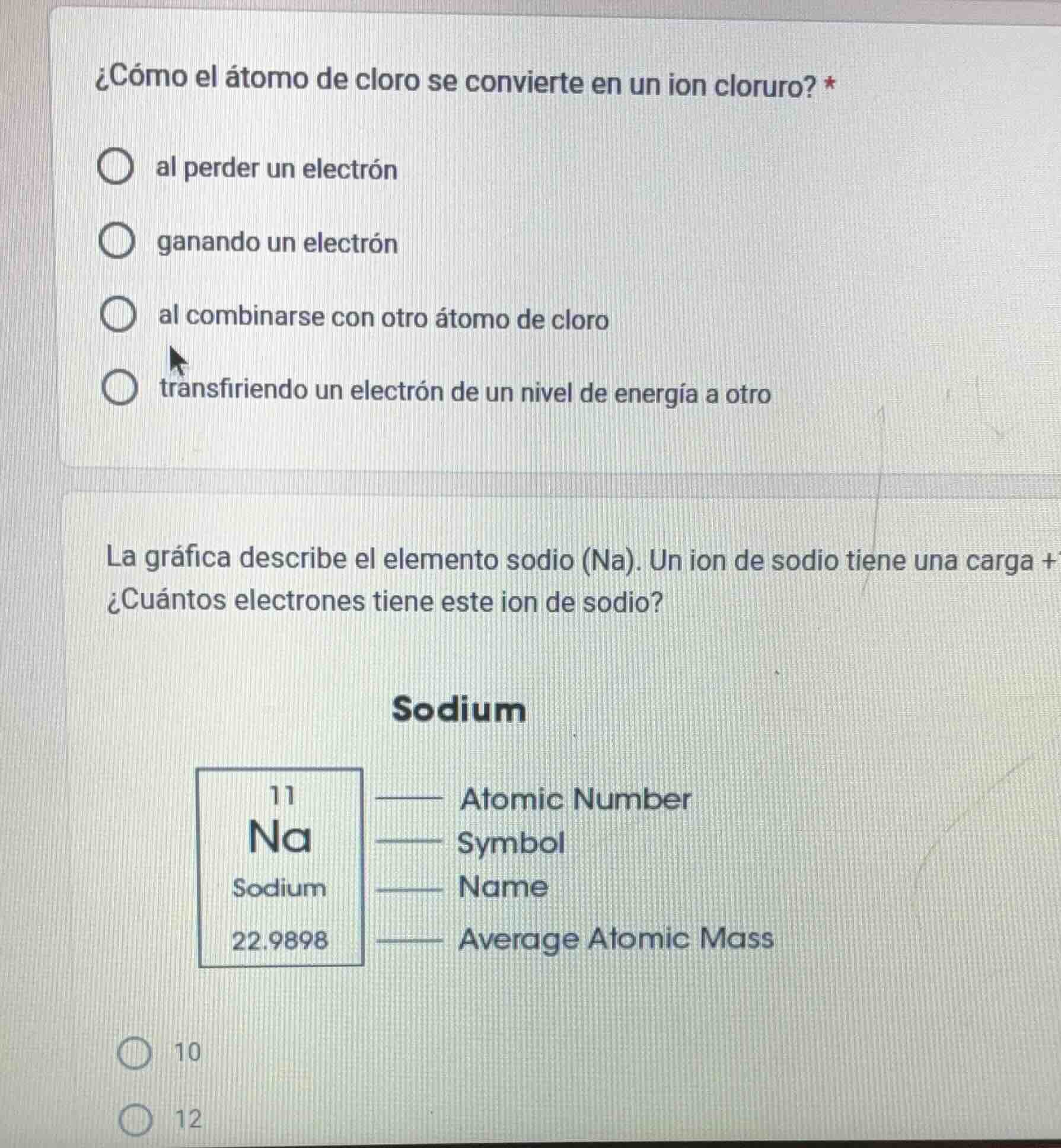
¿cómo el átomo de cloro se convierte en un ion cloruro? *
al perder un electrón
ganando un electrón
al combinarse con otro átomo de cloro
transfiriendo un electrón de un nivel de energía a otro
la gráfica describe el elemento sodio (na). un ion de sodio tiene una carga +
¿cuántos electrones tiene este ion de sodio?
sodium
11
na
sodium
22.9898
atomic number
symbol
name
average atomic mass
10
12
Primera pregunta:
Breves Explicaciones:
El átomo de cloro (Cl) tiene 7 electrones en su nivel de valencia. Para alcanzar la configuración de gas noble (estabilidad), necesita ganar 1 electrón. Al ganar un electrón, el átomo de cloro adquiere una carga negativa (ion cloruro, \( \text{Cl}^- \)). Las otras opciones no son correctas: perder un electrón haría que tuviera carga positiva (lo que no es el cloruro), combinarse con otro cloro forma moléculas, no iones, y transferir electrones entre niveles de energía no forma iones de cloruro.
Respuesta:
B. ganando un electrón
Segunda pregunta:
Explicación:
Paso 1: Recordar la relación entre número atómico y electrones en átomo neutro
El número atómico (Z) de un elemento es igual al número de protones y, en un átomo neutro, también al número de electrones. Para el sodio (Na), el número atómico es 11, por lo que un átomo neutro de Na tiene 11 electrones.
Paso 2: Determinar la carga del ion de sodio
Un ion de sodio (\( \text{Na}^+ \)) tiene una carga +1, lo que significa que ha perdido 1 electrón (ya que la carga positiva se debe a tener más protones que electrones).
Paso 3: Calcular el número de electrones en el ion
Si el átomo neutro tiene 11 electrones y el ion ha perdido 1, entonces el número de electrones en \( \text{Na}^+ \) es \( 11 - 1 = 10 \).
Respuesta:
10
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Primera pregunta:
Breves Explicaciones:
El átomo de cloro (Cl) tiene 7 electrones en su nivel de valencia. Para alcanzar la configuración de gas noble (estabilidad), necesita ganar 1 electrón. Al ganar un electrón, el átomo de cloro adquiere una carga negativa (ion cloruro, \( \text{Cl}^- \)). Las otras opciones no son correctas: perder un electrón haría que tuviera carga positiva (lo que no es el cloruro), combinarse con otro cloro forma moléculas, no iones, y transferir electrones entre niveles de energía no forma iones de cloruro.
Respuesta:
B. ganando un electrón
Segunda pregunta:
Explicación:
Paso 1: Recordar la relación entre número atómico y electrones en átomo neutro
El número atómico (Z) de un elemento es igual al número de protones y, en un átomo neutro, también al número de electrones. Para el sodio (Na), el número atómico es 11, por lo que un átomo neutro de Na tiene 11 electrones.
Paso 2: Determinar la carga del ion de sodio
Un ion de sodio (\( \text{Na}^+ \)) tiene una carga +1, lo que significa que ha perdido 1 electrón (ya que la carga positiva se debe a tener más protones que electrones).
Paso 3: Calcular el número de electrones en el ion
Si el átomo neutro tiene 11 electrones y el ion ha perdido 1, entonces el número de electrones en \( \text{Na}^+ \) es \( 11 - 1 = 10 \).
Respuesta:
10