QUESTION IMAGE
Question
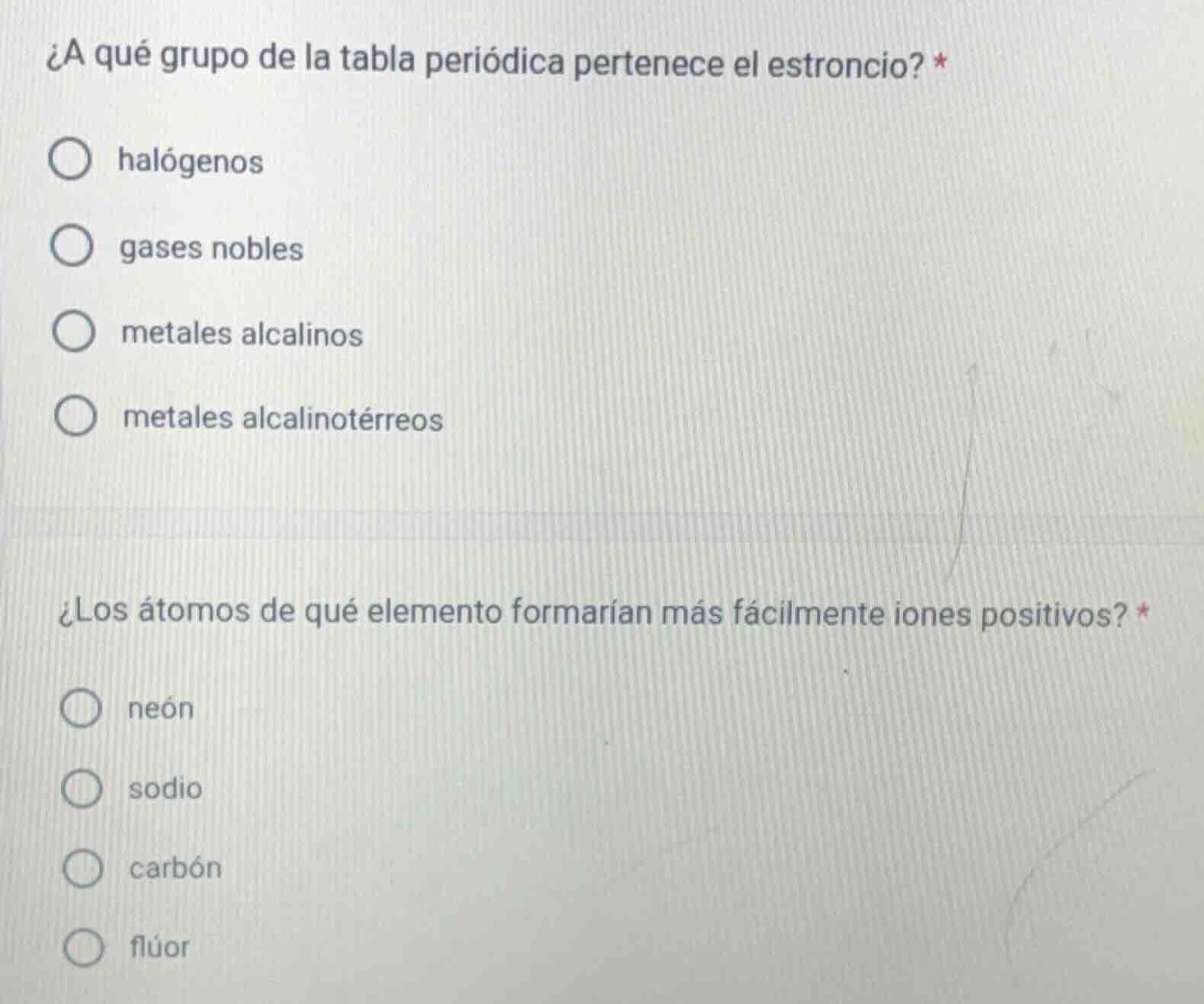
¿a qué grupo de la tabla periódica pertenece el estroncio? *
○ halógenos
○ gases nobles
○ metales alcalinos
○ metales alcalinotérreos
¿los átomos de qué elemento formarían más fácilmente iones positivos? *
○ neón
○ sodio
○ carbón
○ flúor
Primera pregunta:
Breve Explicación:
El estroncio (Sr) tiene número atómico 38 y su configuración electrónica es tal que pertenece al grupo 2 de la tabla periódica. Los metales alcalinotérreos son los del grupo 2, mientras que halógenos son grupo 17, gases nobles grupo 18 y metales alcalinos grupo 1.
Respuesta:
D. metales alcalinotérreos
Segunda pregunta:
Breve Explicación:
Los metales tienden a perder electrones para formar iones positivos. El neón (gas noble) es inerte, el carbono es no metal (tiende a compartir o ganar), el flúor (halógeno) tiende a ganar electrones (ión negativo), y el sodio (metal alcalino, grupo 1) tiene 1 electrón de valencia y pierde fácilmente ese electrón para formar \( \text{Na}^+ \).
Respuesta:
B. sodio
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Primera pregunta:
Breve Explicación:
El estroncio (Sr) tiene número atómico 38 y su configuración electrónica es tal que pertenece al grupo 2 de la tabla periódica. Los metales alcalinotérreos son los del grupo 2, mientras que halógenos son grupo 17, gases nobles grupo 18 y metales alcalinos grupo 1.
Respuesta:
D. metales alcalinotérreos
Segunda pregunta:
Breve Explicación:
Los metales tienden a perder electrones para formar iones positivos. El neón (gas noble) es inerte, el carbono es no metal (tiende a compartir o ganar), el flúor (halógeno) tiende a ganar electrones (ión negativo), y el sodio (metal alcalino, grupo 1) tiene 1 electrón de valencia y pierde fácilmente ese electrón para formar \( \text{Na}^+ \).
Respuesta:
B. sodio