QUESTION IMAGE
Question
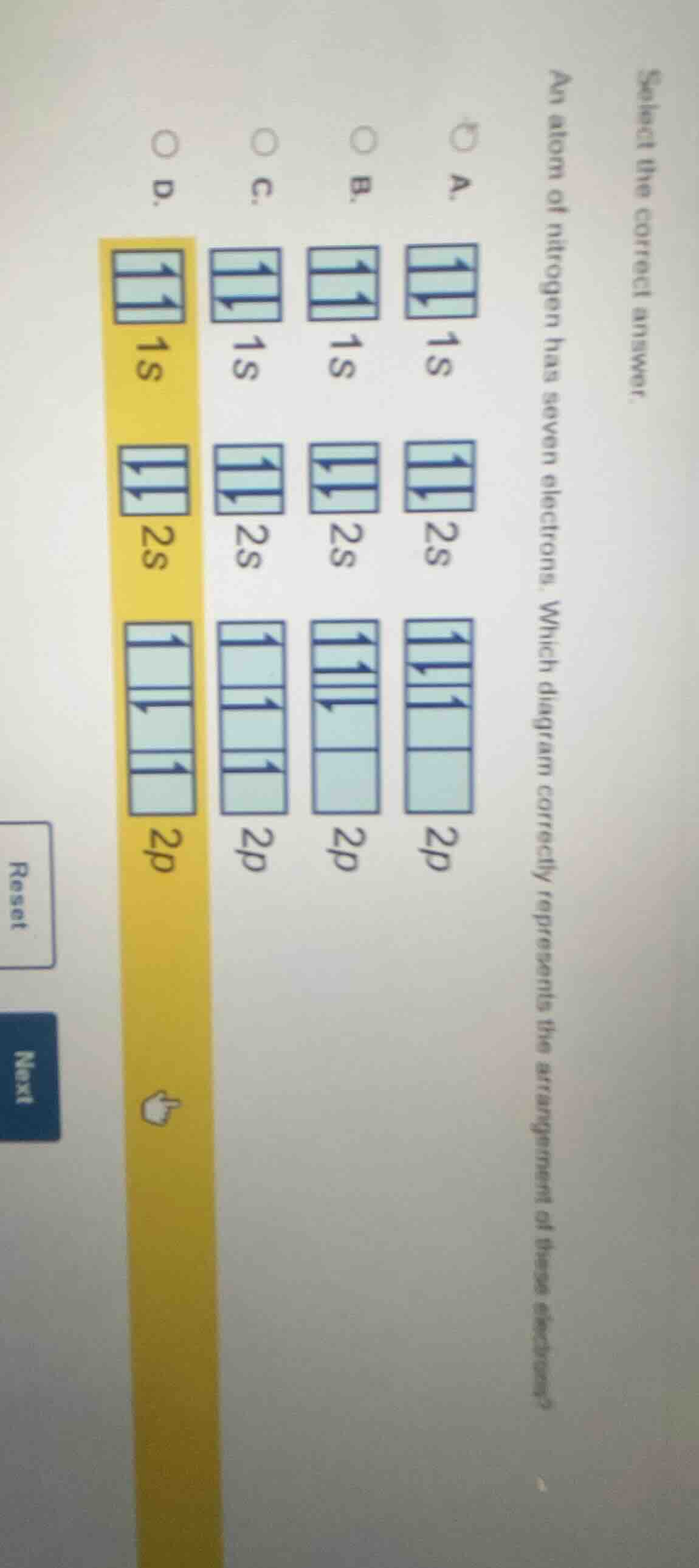
select the correct answer. an atom of nitrogen has seven electrons. which diagram correctly represents the arrangement of these electrons? a. b. c. d.
Step1: Recuerda las reglas de distribución de electrones (principio de exclusión de Pauli, regla de Hund).
El número atómico del nitrógeno es 7, por lo que tiene 7 electrones. La distribución electrónica es \(1s^2 2s^2 2p^3\).
Step2: Analiza los orbitales:
- Orbital \(1s\): 2 electrones (espines opuestos, \(\uparrow\downarrow\)).
- Orbital \(2s\): 2 electrones (espines opuestos, \(\uparrow\downarrow\)).
- Orbital \(2p\): 3 electrones. Según la regla de Hund, los electrones se colocan en orbitales paralelos con espín paralelo antes de emparejar. Entonces, cada uno de los tres orbitales \(2p\) tendrá un electrón con espín en la misma dirección (generalmente \(\uparrow\)) y sin emparejar inicialmente.
Step3: Evalúa las opciones:
- Opción A: En \(2p\) hay electrones emparejados de más, lo que no cumple la regla de Hund para 3 electrones.
- Opción B: En \(2p\) los electrones no siguen la regla de Hund (no están en orbitales separados con espín paralelo).
- Opción C: Verifica la distribución: \(1s\) (\(\uparrow\downarrow\)), \(2s\) (\(\uparrow\downarrow\)), \(2p\) tres electrones en orbitales separados con espín paralelo (cumpliendo regla de Hund y principio de Pauli).
- Opción D: Los espines en \(1s\) o \(2s\) no son opuestos, lo que viola el principio de exclusión de Pauli.
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
C. (La opción C muestra la distribución correcta: \(1s\) con dos electrones opuestos, \(2s\) con dos electrones opuestos y \(2p\) con tres electrones en orbitales separados con espín paralelo, cumpliendo las reglas de distribución electrónica para el nitrógeno.)