QUESTION IMAGE
Question
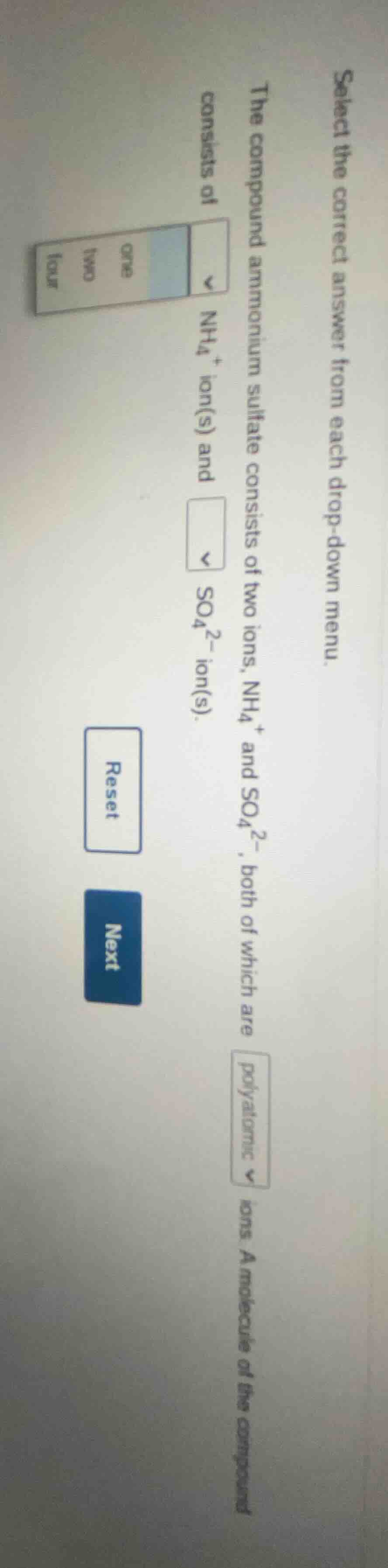
select the correct answer from each drop - down menu.
the compound ammonium sulfate consists of two ions, $nh_4^+$ and $so_4^{2 - }$, both of which are polyatomic ions. a molecule of the compound consists of $nh_4^+$ ion(s) and $so_4^{2 - }$ ion(s).
Step1: Analizar la fórmula del sulfato de amonio
La fórmula del sulfato de amonio es \((NH_4)_2SO_4\). Para determinar el número de iones \(NH_4^+\) y \(SO_4^{2-}\), se considera la carga y la neutralidad de la molécula.
Step2: Determinar el número de iones \(NH_4^+\)
La carga del ion \(SO_4^{2-}\) es -2. Para neutralizar esta carga, se necesitan dos iones \(NH_4^+\) (cada uno con carga +1), ya que \(2\times(+1) + (-2) = 0\). Entonces, el número de iones \(NH_4^+\) es dos.
Step3: Determinar el número de iones \(SO_4^{2-}\)
En la fórmula \((NH_4)_2SO_4\), hay un solo ion \(SO_4^{2-}\) por molécula del compuesto.
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Para el primer menú desplegable (número de \(NH_4^+\) iones): dos
Para el segundo menú desplegable (número de \(SO_4^{2-}\) iones): uno