QUESTION IMAGE
Question
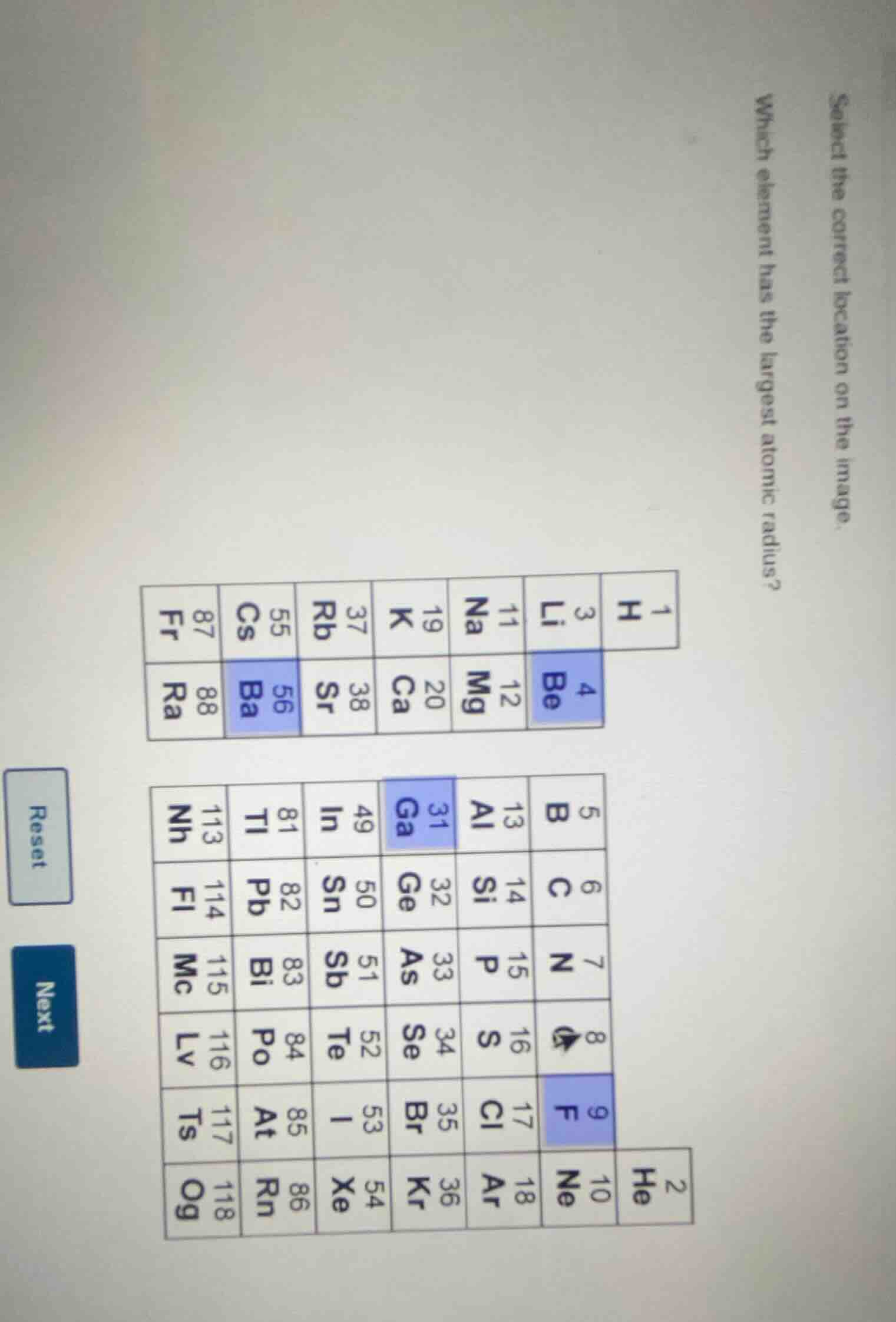
select the correct location on the image. which element has the largest atomic radius?
Step1: Recuerda la tendencia del radio atómico
El radio atómico aumenta hacia abajo en un grupo y hacia la izquierda en un período. Esto se debe a que al bajar un grupo, se agregan niveles de energía (capas electrónicas), lo que aumenta el tamaño del átomo. Al avanzar hacia la izquierda en un período, la carga nuclear efectiva es menor, por lo que los electrones están menos atrapados y el átomo es más grande.
Step2: Analiza la ubicación de los elementos
Mirando la tabla periódica proporcionada, los elementos del grupo 1 (alcalinos) son H, Li, Na, K, Rb, Cs, Fr. Los del grupo 2 son Be, Mg, Ca, Sr, Ba, Ra. Los del grupo 13 a 18 son los demás.
Entre los elementos mostrados, Fr (francio) está en el grupo 1 y en la última fila (mayor número atómico, más abajo en el grupo). Comparando con Cs (cesio), Rb (rubidio), K (potasio), Na (sodio), Li (litio) y H (hidrógeno), Fr está más abajo en el grupo 1.
También, comparando con elementos de otros grupos, como Ra (radón? No, Ra es radio, grupo 2), pero el grupo 1 tiene átomos más grandes que el grupo 2 en la misma fila porque tienen menos electrones en la valencia y menor carga nuclear efectiva.
Step3: Determina el elemento con mayor radio
Dado que el radio atómico aumenta hacia abajo en un grupo y Fr es el elemento del grupo 1 más abajo en la tabla (número atómico 87), tiene más capas electrónicas que los otros alcalinos y, por lo tanto, el radio atómico más grande.
Snap & solve any problem in the app
Get step-by-step solutions on Sovi AI
Photo-based solutions with guided steps
Explore more problems and detailed explanations
Fr (87) (el elemento con símbolo Fr y número atómico 87)